Nội dung sản phẩm
Chúng tôi mong muốn hiển thị cho bạn thông tin sản phẩm chính xác. Nội dung, các nhà sản xuất và những gì cung cấp bạn thấy ở đây và chúng tôi chưa xác minh điều đó. Từ chối trách nhiệm
Thành phần
Mỗi viên Viên nén chứa:
| Thông tin thành phần | Hàm lượng |
|---|---|
| Tenofovir Alafenamide | 25mg |
Công dụng (Chỉ định)
Thuốc Hepbest 25mg được chỉ định dùng trong trường hợp sau:
- Tenofovir Alafenamide được chỉ định điều trị nhiễm virus viêm gan B mạn tính ở bệnh nhân xơ gan còn bù.
Cách dùng & Liều dùng
Cách dùng Hepbest 25mg
- Uống cả viên thuốc với nước, nên uống thuốc trong bữa ăn.
Liều dùng Hepbest 25mg
- Trước khi bắt đầu điều trị với Tenofovir Alafenamide, nên xác định xem bệnh nhân có nhiễm HIV – 1 không. Alafenamide đơn trị không nên sử dụng cho bệnh nhân nhiễm HIV – 1.
- Nên xét nghiệm nồng độ creatinine huyết thanh, phospho huyết, độ thanh thải creatinin, glucose niệu, protein niệu trước và trong khi điều trị với Tenofovir Alafenamide.
- Liều khuyến cáo là 1 viên 25 mg, 1 lần/ngày, uống kèm hoặc không kèm thức ăn.
- Không cần chỉnh liều ở người cao tuổi trên 65 tuổi.
- Không cần chỉnh liều ở bệnh nhân suy thận nhẹ và vừa. Không khuyến cáo dùng thuốc cho bệnh nhân suy thận giai đoạn cuối (ClCr < 15 ml/phút). Ở bệnh nhân cần thẩm phân máu, dùng Tenofovir Alafenamide sau khi quá trình thẩm phân kết thúc.
- Không cần chỉnh liều ở bệnh nhân suy gan nhẹ (Child – Pugh A). Thuốc không khuyến cáo dùng cho bệnh nhân xơ gan mất bù (Child – Pugh B, C).
- Hiệu quả và an toàn của thuốc chưa được nghiên cứu ở trẻ dưới 18 tuổi.
Lưu ý: Liều dùng trên chỉ mang tính chất tham khảo. Liều dùng cụ thể tùy thuộc vào thể trạng và mức độ diễn tiến của bệnh. Để có liều dùng phù hợp, bạn cần tham khảo ý kiến bác sĩ hoặc chuyên viên y tế.
Quá liều
- Nếu quá liều xảy ra, theo dõi bệnh nhân về các dấu hiệu của nhiễm độc tenofovir. Các biện pháp hỗ trợ chung bao gồm theo dõi dấu hiệu sinh tồn cũng như tình trạng lâm sàng của bệnh nhân. Tenofovir có thể được loại trừ hiệu quả bằng thẩm phân máu với hệ số thẩm phân xấp xỉ 54%.
Làm gì khi quên 1 liều?
- Nếu quên dùng một liều thuốc, hãy uống càng sớm càng tốt khi nhớ ra. Tuy nhiên, nếu gần với liều kế tiếp, hãy bỏ qua liều đã quên và uống liều kế tiếp vào thời điểm như kế hoạch. Không uống gấp đôi liều đã quy định.
Chống chỉ định
Thuốc Hepbest 25mg chống chỉ định trong các trường hợp sau:
- Mẫn cảm với các thành phần của thuốc.
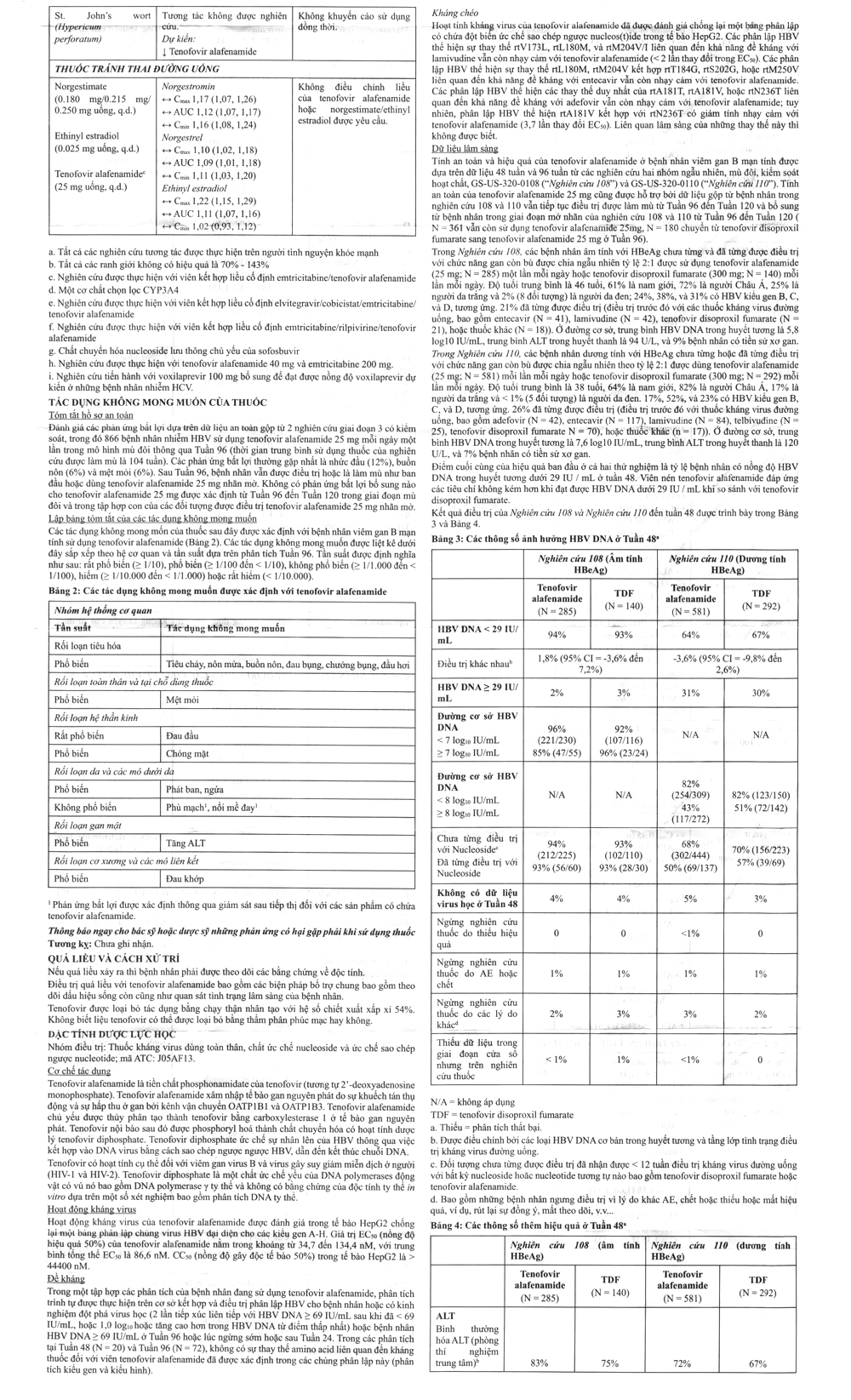
Tác dụng phụ
Khi sử dụng thuốc Hepbest 25mg, bạn có thể gặp các tác dụng không mong muốn (ADR).
Thường gặp, ADR > 1/100
- Hệ thần kinh: Đau đầu.
- Hệ tiêu hóa: Buồn nôn, nôn, tiêu chảy, đau bụng, đầy hơi.
- Toàn thân: Mệt mỏi.
- Da: Phát ban.
- Cơ xương: Đau lưng.
- Gan: Tăng men gan (ALT, AST).
- Rối loạn lipid máu: Tăng LDL – cholesterol.
Hướng dẫn cách xử trí ADR
- Khi gặp tác dụng phụ của thuốc, cần ngưng sử dụng và thông báo cho bác sĩ hoặc đến cơ sở y tế gần nhất để được xử trí kịp thời.
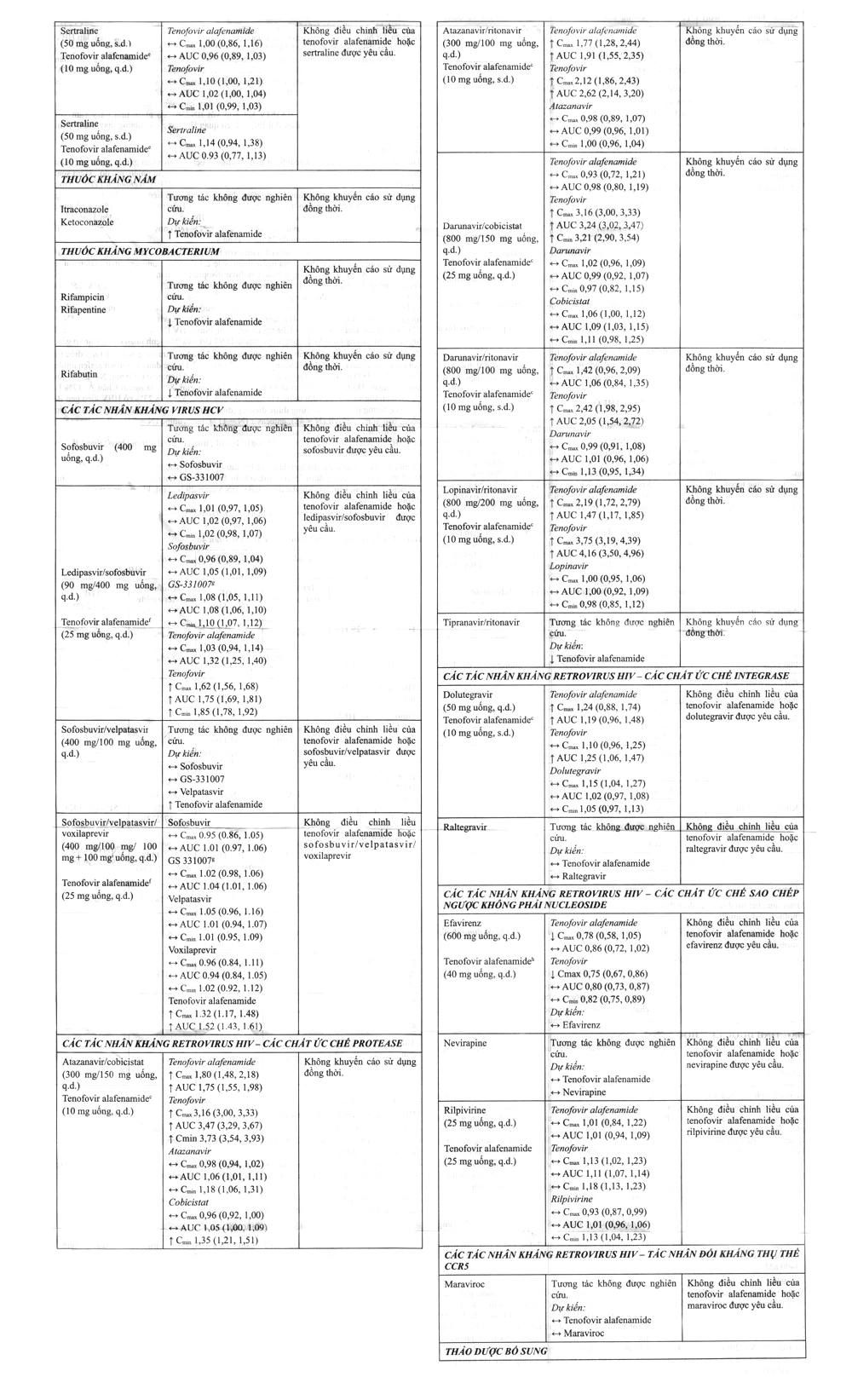
Tương tác thuốc
- Tenofovir Alafenamide là chất nền của P – glycoprotein (P – gp) và BCRP. Những thuốc cảm ứng hoạt động của P – gp làm giảm hấp thu và làm giảm nồng độ Tenofovir Alafenamide trong máu, ảnh hưởng đến hiệu quả điều trị. Các thuốc ức chế hoạt động P – gp và BCRP làm tăng nồng độ Tenofovir Alafenamide trong máu, làm tăng độc tính.
- Tenofovir bài tiết chủ yếu qua thận (qua lọc cầu thận và bài tiết tích cực ở ống thận). Dùng phối hợp với các thuốc làm giảm hoạt động của thận hoặc cạnh tranh bài tiết tích cực ở ống thận (acyclovir, cidofovir, ganciclovir, valacyclovir, valganciclovir, aminoglycoside, liều cao NSAIDs…) có thể làm tăng nồng độ tenofovir trong máu, dẫn đến tăng độc tính.
- Thuốc chống động kinh (carbamazepine, oxcarbazepine, phenobarbital, phenytoin), thuốc kháng lao (rifabutin, rifampin), St. John’s Wort làm giảm nồng độ Tenofovir Alafenamide trong máu. Nên tăng liều Tenofovir Alafenamide thành 2 viên 25 mg/ngày khi phối hợp với carbamazepine. Các phối hợp còn lại không được khuyến cáo.
- Không dùng Hepbest 25 mg chung với các thuốc có chứa tenofovir alafenamide, tenofovir disoproxil fumarate, adenovir dipivoxil.
Lưu ý (Thận trọng khi sử dụng)
- Đã có báo cáo về nhiễm toan lactic và gan to nghiêm trọng kèm nhiễm mỡ, có trường hợp tử vong khi sử dụng các chất tương tự nucleoside (tenofovir disoproxil fumarate…) phối hợp với thuốc kháng retrovirus. Phần lớn trường hợp này là ở phụ nữ. Béo phì và phơi nhiễm nucleoside kéo dài là các yếu tố nguy cơ.
- Cần thận trọng khi dùng các chất tương tự nucleoside, đặc biệt ở bệnh nhân có các yếu tố nguy cơ mắc bệnh về gan. Ngưng Tenofovir Alafenamide ở bệnh nhân có dấu hiệu lâm sàng hoặc xét nghiệm gợi ý nhiễm toan lactic hay nhiễm độc gan rõ rệt (có thể bao gồm gan to và nhiễm mỡ cả khi không tăng transaminase rõ rệt).
- Ngưng điều trị chống viêm gan B có thể dẫn đến đợt cấp nghiêm trọng viêm gan B. Sau khi ngưng dùng Tenofovir Alafenamide, bệnh nhân nên được theo dõi kỹ các dấu hiệu lâm sàng và xét nghiệm thường xuyên trong ít nhất vài tháng. Nếu cần thiết, phải tiếp tục điều trị viêm gan B.
- Do nguy cơ phát triển đề kháng HIV – 1, không khuyến cáo dùng Tenofovir Alafenamide đơn trị ở bệnh nhân nhiễm HIV – 1. Tính an toàn và hiệu quả của thuốc chưa được thiết lập ở bệnh nhân đồng nhiễm HBV và HIV – 1. Nên xét nghiệm kháng thể kháng HIV trước khi sử dụng thuốc này cho bệnh nhân nhiễm HBV, nếu dương tính với HIV, khuyến cáo dùng phác đồ kết hợp thuốc kháng retrovirus.
- Suy thận (bao gồm suy thận cấp và hội chứng Fanconi – tổn thương ống thận kèm giảm phospho huyết nặng) đã được báo cáo khi sử dụng tiền dược tenofovir in vivo và trong thử nghiệm ở người. Trên lâm sàng, Tenofovir Alafenamide không gây các tác dụng không mong muốn này.
- Ở bệnh nhân sử dụng tiền dược tenofovir và các thuốc độc thận khác (NSAIDs…) làm tăng nguy cơ suy giảm chức năng thận.
- Nên xét nghiệm nồng độ creatinine huyết thanh, phospho huyết, độ thanh thải creatinin, glucose niệu, protein niệu trước và trong khi điều trị với Tenofovir Alafenamide.
Khả năng lái xe và vận hành máy móc
- Chưa có báo cáo.
Thời kỳ mang thai
- Không có dữ liệu đầy đủ trên phụ nữ có thai. In vivo, không có tác dụng bất lợi trên sự phát triển các cơ quan của thai nhi khi sử dụng liều khuyến cáo Tenofovir Alafenamide dài ngày (lên đến 51 lần). Không thấy ảnh hưởng đến bào thai ở chuột và thỏ khi sử dụng liều hàng ngày Tenofovir Alafenamide.
Thời kỳ cho con bú
- Chưa rõ Tenofovir Alafenamide và chất chuyển hóa của nó có qua được sữa mẹ, có ảnh hưởng đến sự sản xuất sữa ở người hay ảnh hưởng trẻ bú mẹ không. Tuy nhiên, đã có nghiên cứu thuốc có bài tiết qua sữa chuột và khỉ.
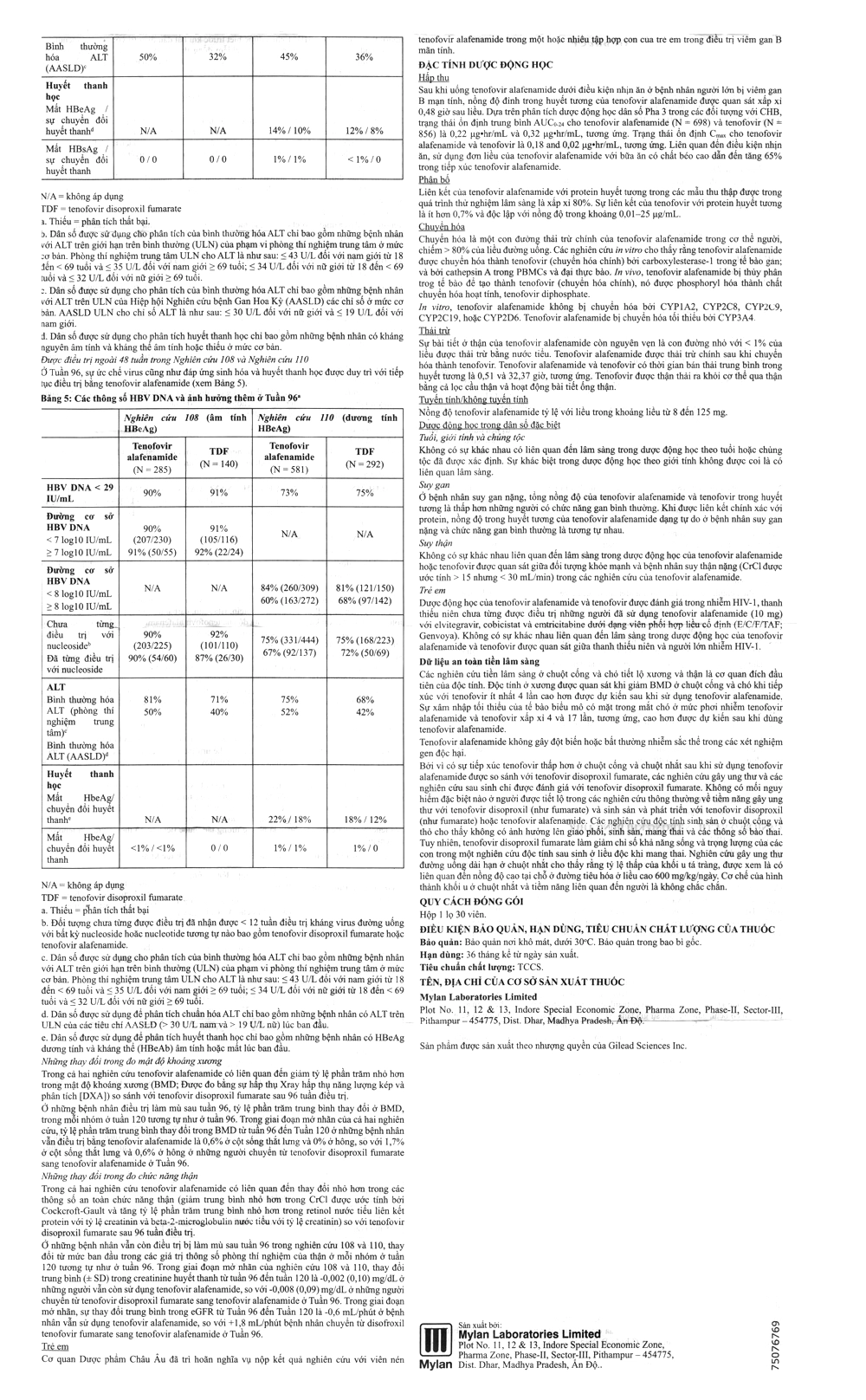
Dược động học (Tác động của cơ thể với thuốc)
Hấp thu
- Tenofovir alafenamide là tiền chất phosphonamidate của tenofovir.
- Sau khi uống, nồng độ đỉnh trong huyết tương đạt được sau khoảng 0,5 giờ.
- Dùng thuốc cùng bữa ăn giàu chất béo làm tăng sinh khả dụng gấp 1,65 lần so với trạng thái bụng đói.
- Suy gan nhẹ (Child-Pugh: A): Sự hiện diện trong huyết tương của tenofovir alafenamide và tenofovir lần lượt giảm 7,5 và 11% so với những người có chức năng gan bình thường.
- Suy thận nặng: Sự hiện diện trong huyết tương của tenofovir alafenamide và tenofovir cao hơn lần lượt 1,9 và 5,7 lần so với những người có chức năng thận bình thường.
Phân bố
- Tỷ lệ thuốc gắn với protein huyết tương là 80%.
Chuyển hóa
- Tenofovir alafenamide trải qua quá trình thủy phân ban đầu thành tenofovir và sau đó được phosphoryl hóa bởi các enzym tế bào tạo thành tenofovir diphosphat hoạt động.
- Chỉ được chuyển hóa một phần nhỏ bởi CYP3A.
Thải trừ
- Thải trừ qua thận thông qua cơ chế lọc tại cầu thận và bài tiết tích cực tại ống thận.
- 32% liều dùng thải trừ qua phân; <1% thải trừ qua nước tiểu.
Dược lực học (Tác động của thuốc lên cơ thể)
- Chất kháng virus ức chế men sao chép ngược nucleotide.
- Tenofovir alafenamide đi vào tế bào gan sơ cấp bằng cách khuếch tán thụ động và bằng protein vận chuyển anion hữu cơ (organic anion transport protein-OATP) 1B1 và 1B3.
- Được chuyển đổi thành tenofovir trong tế bào gan thông qua quá trình thủy phân (chủ yếu bởi CES1) và sau đó được phosphoryl hóa bởi các kinase của tế bào thành tenofovir diphosphat.
- Cũng được chuyển đổi thành tenofovir trong tế bào máu đơn nhân ngoại vi (peripheral blood mononuclear cells – PBMCs) và đại thực bào thông qua thủy phân bởi cathepsin A và sau đó được phosphoryl hóa bởi các kinase của tế bào thành tenofovir diphosphat.
- Hoạt tính chống lại HBV; cũng có hoạt tính chống lại HIV-1 và có một số hoạt tính in vitro chống lại HIV-2.
- Tenofovir diphosphat ức chế sự sao chép của HBV thông qua sự gắn vào DNA của virus bởi men sao chép ngược, dẫn đến kết thúc chuỗi DNA. Ức chế yếu các polymerase DNA của động vật có vú (bao gồm DNA polymerase γ của ty thể); không có bằng chứng về độc tính đối với ti thể trong nuôi cấy tế bào.
- Các chủng HBV phân lập kháng với một số thuốc kháng virus ức chế men sao chép ngược nucleoside hoặc nucleotide khác được sử dụng để điều trị nhiễm HBV (ví dụ, adefovir, entecavir, lamivudine) cũng có thể làm giảm tính nhạy cảm với tenofovir.
Bảo quản
- Tránh ánh nắng trực tiếp
- Để xa tầm tay trẻ em
Hạn dùng
24 tháng kể từ ngày sản xuất
Bài viết được cập nhật lần cuối 14 Tháng 9, 2024
Thông tin thương hiệu

Mylan
Giới thiệu về Mylan
Mylan là một trong những tập đoàn dược phẩm hàng đầu thế giới, chuyên nghiên cứu, sản xuất và phân phối thuốc generic cũng như các loại thuốc đặc trị. Công ty có trụ sở chính tại Canonsburg, Pennsylvania, Hoa Kỳ, và hoạt động tại hơn 165 quốc gia trên toàn cầu.
Mylan cam kết cung cấp các loại thuốc chất lượng cao với giá cả phải chăng, giúp bệnh nhân trên khắp thế giới tiếp cận các phương pháp điều trị tiên tiến. Công ty không ngừng đổi mới để mang đến các giải pháp y tế hiệu quả cho những bệnh lý phức tạp.
Lịch sử hình thành và phát triển
- 1961: Thành lập tại White Sulphur Springs, West Virginia, Hoa Kỳ, với tư cách là nhà phân phối thuốc
- 1966: Bắt đầu sản xuất dược phẩm, mở rộng danh mục sản phẩm
- 2007: Mua lại Matrix Laboratories Limited (Ấn Độ) và bộ phận thuốc generic của Merck KGaA (Đức), giúp mở rộng thị phần toàn cầu
- 2016: Đối mặt với tranh cãi về giá EpiPen, cam kết cải thiện khả năng tiếp cận thuốc cho bệnh nhân
- 2020: Hợp nhất với Upjohn, bộ phận thuốc generic của Pfizer, để thành lập Viatris – một công ty chăm sóc sức khỏe toàn cầu mới
Thế mạnh của Mylan
Danh mục sản phẩm đa dạng
- Thuốc generic: Hỗ trợ điều trị tim mạch, tiểu đường, ung thư, rối loạn thần kinh và các bệnh truyền nhiễm
- Thuốc đặc trị: Gồm các loại thuốc chuyên biệt điều trị HIV/AIDS, viêm gan C và ung thư
- Dược phẩm sinh học: Cung cấp các liệu pháp sinh học nhằm thay thế thuốc biệt dược có giá thành cao
Công nghệ và nghiên cứu tiên tiến
- Đầu tư mạnh vào R&D, phát triển công nghệ sản xuất tiên tiến
- Hệ thống nhà máy đạt chuẩn GMP, đảm bảo chất lượng dược phẩm
- Ứng dụng công nghệ sinh học trong nghiên cứu thuốc generic phức tạp
Cam kết phát triển bền vững
- Tăng cường khả năng tiếp cận thuốc cho bệnh nhân trên toàn cầu
- Hợp tác với WHO và các tổ chức y tế để cải thiện sức khỏe cộng đồng
- Áp dụng quy trình sản xuất thân thiện với môi trường, giảm thiểu tác động đến khí hậu
Thành tựu nổi bật
- Một trong những công ty dược phẩm generic lớn nhất thế giới
- Đóng vai trò quan trọng trong việc cung cấp thuốc điều trị HIV/AIDS giá rẻ cho các nước đang phát triển
- Được xếp hạng cao trong danh sách các công ty dược phẩm có ảnh hưởng toàn cầu
Thông tin liên hệ
- Trụ sở chính: 1000 Mylan Boulevard, Canonsburg, Pennsylvania, Hoa Kỳ
- Website: www.viatris.com (sau khi hợp nhất với Upjohn)
- Điện thoại: +1-724-514-1800
Mylan, nay là một phần của Viatris, tiếp tục sứ mệnh cung cấp các giải pháp y tế chất lượng cao, giúp hàng triệu bệnh nhân trên thế giới có cơ hội điều trị hiệu quả và tiết kiệm chi phí.


























 - Thư viện thông tin cho dược sĩ và người dùng
- Thư viện thông tin cho dược sĩ và người dùng